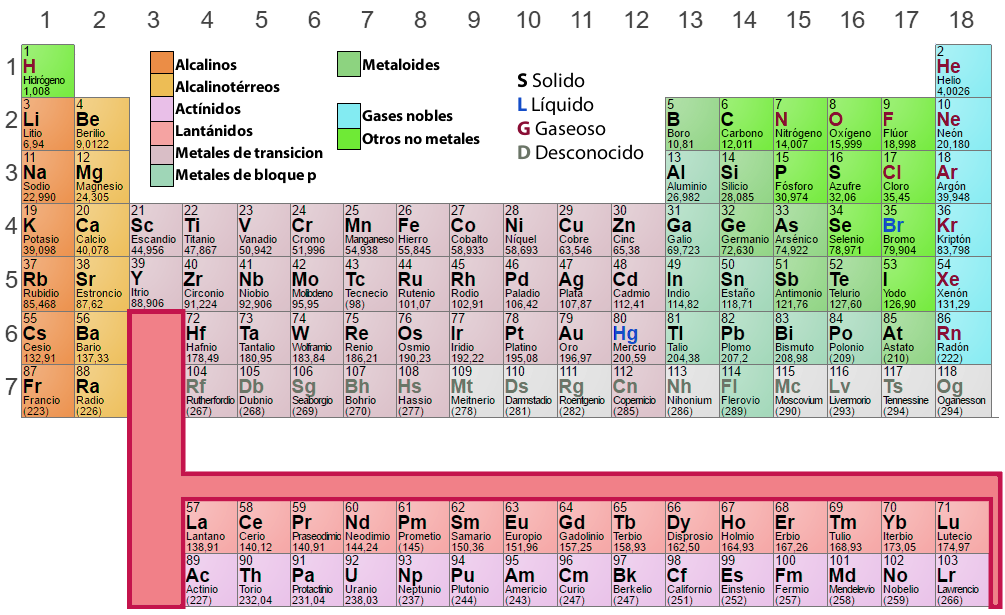
La tabla periódica es uno de los símbolos más emblemáticos de la ciencia, en ella se resumen muchos de los conocimientos de la química. En cualquiera de sus versiones está presente en aulas y laboratorios del mundo. Ninguna otra disciplina cuenta con un documento parecido.
El sistema periódico desarrollado en la segunda mitad del siglo XIX, proporcionó una ordenación sistemática de los elementos en grupos naturales. El alcance de esta ordenación permitió predecir con bastante certeza las propiedades de algunos elementos desconocidos y los probables compuestos que formaban. Desarrollos posteriores proporcionaron la base teórica de la Tabla Periódica actual. El gran número de elementos conocidos y sustancias sintetizadas generó la necesidad urgente de clasificarlos.
En la tabla periódica, los elementos que tienen un patrón similar de configuración de los electrones de la capa externa están dispuestos en las mismas columnas, llamados Grupos o Familias. Existen 18 grupos, a los que se le adiciona una letra (A ó B). Aquellos átomos indicados con letra A, corresponden a elementos cuyo electrón diferencial se encuentra en los orbitales s ó p. Los átomos, a los que se le asigna la letra B, son aquellos cuyo electrón diferencial se ubica en los orbitales d ó f.
Los átomos con igual número de niveles energéticos se encuentran en las mismas filas (periodos). Cada período comienza con un metal alcalino y concluye con un gas noble, a excepción del período 1.
Fecha de Actualización : 26 de Junio 2017